铜作为人类必需的微量营养元素,是多种蛋白或酶的辅因子,广泛参与关键的生命进程。相关研究表明,非酒精性脂肪肝(NAFLD)的发生、发展,通常伴随血清与组织的铜水平异常下调;适量补充机体的铜元素有望延缓脂肪肝进程。正常条件下,细胞的铜摄入受限于细胞膜的金属还原酶与金属转运蛋白,小分子铜载体可大幅提升细胞的铜载入效率,即胞外铜配位-胞内铜释放。另一方面,天然黄酮醇具有良好的生物活性,可用于NAFLD干预或联合治疗。因此,整合黄酮醇生物活性与适量铜载入,有望作为NAFLD协同干预的有效策略。
研究者将8-羟基喹啉衍生基团用于替换天然黄酮醇的B环结构,改造天然黄酮的铜配位中心,构建铜转运效率更高的铜离子载体,即HQFs系列分子;这类结构不仅保持天然黄酮醇的分子骨架,也将配位中心由氧原子拓展至喹啉中心,具备适中的铜配位能力(图1)。研究表明,HQFs自身的毒副作用较低、铜转运效率高、具备类似黄酮的生物活性;在NAFLD的细胞和动物模型中,HQF介导的铜载入展示出良好的脂代谢调控效果。
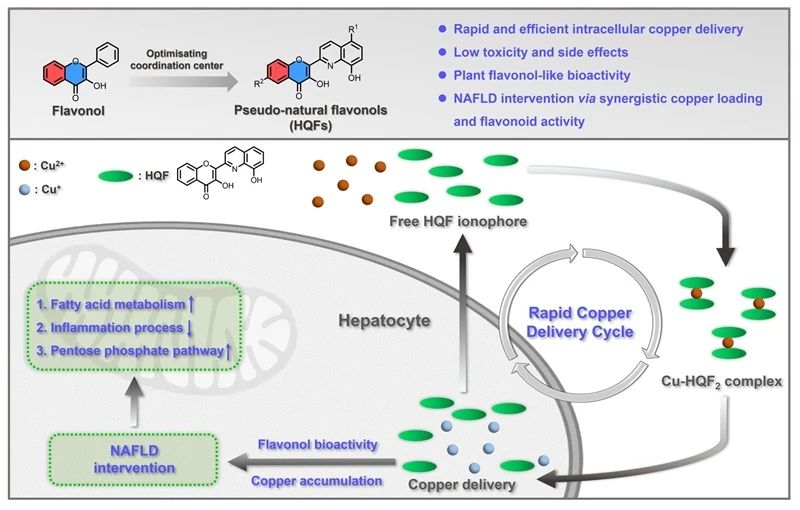
图1. 黄酮醇类铜离子载体设计思路与脂肪肝干预示意图。
基于转录组学与代谢组学分析,研究者推测NAFLD干预机制可能涉及多个脂代谢基因的表达上调、炎症进程与磷酸戊糖途径的动态变化;其中,线粒体P450相关因子、JAK-STAT通路可能具有潜在效应。在NAFLD模型细胞中,成功验证HQF与铜载入对细胞的降脂具有协同效应,且MT1X、MT1E、STEAP4的差异表达表明铜有效摄入、扰动胞内铜稳态。研究者在高脂饮食的小鼠模型中(图2),系统性表征HQF介导的适量铜摄入,高效调控肝脏脂滴水平、延缓肝损伤;生理指标的各项数据表明,肝脏脂代谢受显著干预,且对其它组织与血液指标无明显干扰。本研究开发的新型铜离子载体有望用于辅助细胞或机体的铜载入,调控相关的疾病进程;例如,促进癌细胞铜摄入激活“铜死亡”进程,实现高效抗癌等。
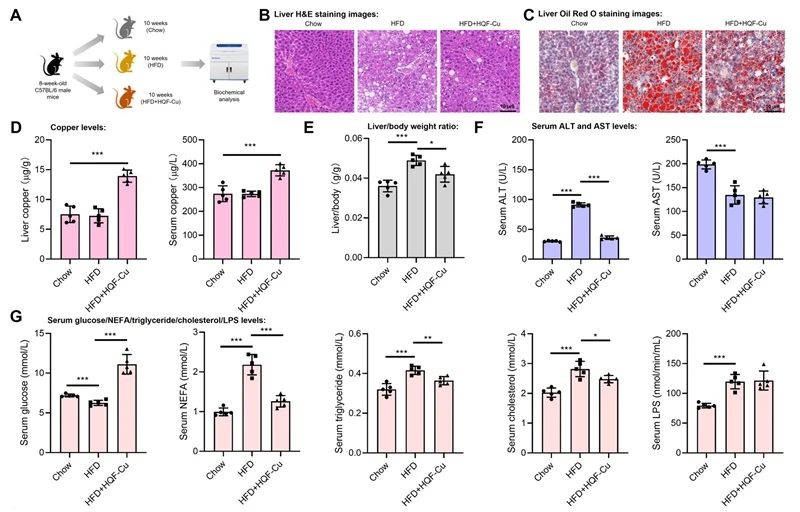
图2. 小鼠模型中,黄酮醇类载体介导的铜载入高效干预脂肪肝。
该成果于近日发表于药物化学领域顶级期刊Journal of Medicinal Chemistry,湖北大学李享与王凯、东北林业大学邱爽为该论文共同通讯作者,湖北大学姜军与陈钢、迈维代谢张卫琴为论文共同第一作者。同时,重庆医科大学附属第三医院秦思、湖北科技学院李满等人对本研究亦具有较大贡献。
文章转自微信公众号“X-MOL咨询”
(审稿:王凯)